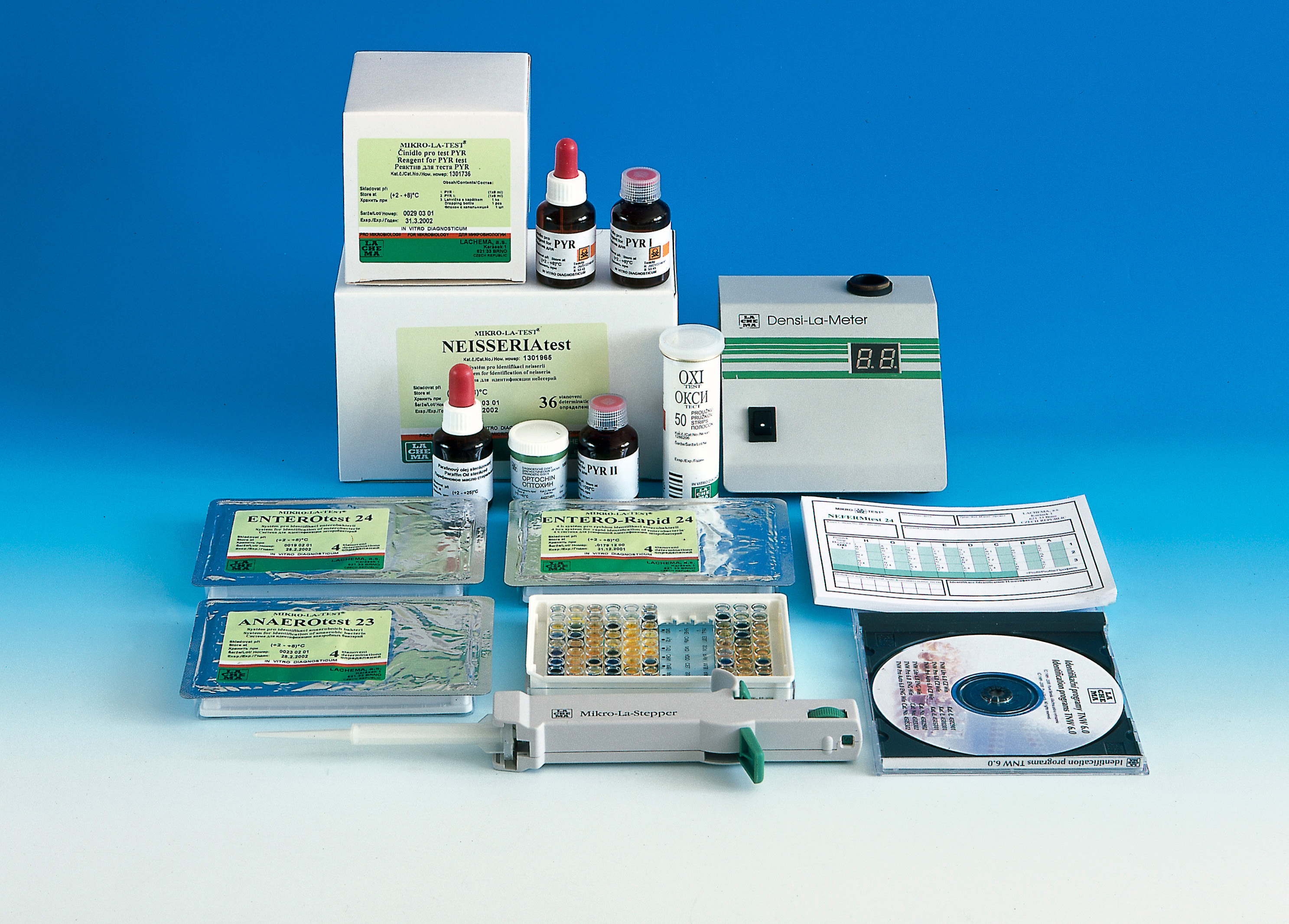
 Постановлением Кабинета Министров от 22 декабря 2014 года № 352 утверждено Положение о порядке регистрации лекарственных средств и изделий медицинского назначения и выдачи регистрационного удостоверения.
Постановлением Кабинета Министров от 22 декабря 2014 года № 352 утверждено Положение о порядке регистрации лекарственных средств и изделий медицинского назначения и выдачи регистрационного удостоверения.
Регистрация и выдача регистрационного удостоверения на лекарственное средство и изделие медицинского назначения осуществляются Главным управлением по контролю качества лекарственных средств и медицинской техники Министерства здравоохранения.
Регистрация предусматривает выдачу субъектам предпринимательства - юридическим лицам - регистрационного удостоверения лекарственного средства и изделия медицинского назначения, которое является основанием для их применения в медицинской практике. Срок действия удостоверения - 5 лет.
В случае изменения сведений, приведенных в регистрационных документах лекарства и медицинского изделия, в период действия удостоверения на основании представленных субъектом предпринимательства в Главное управление заявления и документов, касающихся изменений, в регистрационные документы лекарственного средства и изделия медицинского назначения вносятся соответствующие изменения и дополнения.
Документ регулирует также регистрацию и выдачу регистрационного удостоверения на зарубежное лекарственное средство и изделие медицинского назначения.
К разрешительным требованиям и условиям, обязательным к выполнению субъектом предпринимательства при применении в медицинской практике лекарства и медицинского изделия относятся:
безусловное соблюдение субъектами предпринимательства законодательных актов при их применении в медицинской практике;
представление в Главное управление владельцем удостоверения исчерпывающей информации об изменениях и дополнениях в регистрационные документы, с изложением полных сведений о причине внесения изменений, их влиянии на эффективность, безопасность и показатели качества лекарства и медицинского изделия, включая обязательное регулярное оповещение Главного управления о новых данных относительно их фармакологической эффективности и безопасности;
обязательное соблюдение данных, приведенных в регистрационных документах лекарств и медицинских изделий;
своевременное устранение недостатков, указанных экспертами, а также представление образцов лекарств, медицинских изделий и других материалов в установленные сроки.
Для получения регистрационного удостоверения субъект предпринимательства (или доверенное лицо, действующее от его имени) представляет утвержденный перечень документов. Требовать от субъекта предпринимательства представления иных документов и образцов не разрешается.
Документы и соответствующие образцы, необходимые для получения регистрационного удостоверения, представляются в Главное управление нарочно, через средства почтовой связи или в электронной форме, подписанные электронной цифровой подписью субъекта предпринимательства с уведомлением об их получении. При этом образцы представляются нарочно или через средства почтовой связи.
Принятие документов подтверждается описью, которая незамедлительно выдается (направляется) субъекту предпринимательства с отметкой о дате приема документов, указанием должности, фамилии, имени и подтверждается подписью лица, принявшего документы.
Главному управлению запрещено разглашать конфиденциальные сведения, приведенные в документах, представленных для получения удостоверения.
Сбор за рассмотрение заявления о выдаче регистрационного удостоверения не подлежит возврату в случае отказа субъекта предпринимательства от поданного заявления.
Срок рассмотрения заявления о выдаче удостоверения не может превышать 180 рабочих дней с даты приема заявления. Однако, в указанный срок не включаются:
срок, не превышающий 45 рабочих дней, установленный для устранения недостатков, выявленных в процессе экспертизы лекарства и медицинского изделия, и представления соответствующих документов заявителем;
срок, не превышающий 45 рабочих дней, установленный для представления заявителем в базы программ клинических испытаний, образцов лекарств и медицинского изделия, согласованных в соответствующем порядке для проведения клинических испытаний;
сроки проведения клинических испытаний.
Не позднее 1 рабочего дня с даты принятия соответствующего решения Главное управление должно выдать субъекту предпринимательства регистрационное удостоверение или уведомить его в письменной форме об отказе в выдаче такого документа.
Основания для отказа в выдаче регистрационного удостоверения:
представление документов не в полном объеме;
несоответствие субъекта предпринимательства разрешительным требованиям и условиям;
наличие в документах недостоверных или искаженных сведений;
получение обоснованного отрицательного заключения по итогам изучения, исследований, проверок (обследований) или иных научно-технических оценок (экспертизы регистрационных документов лекарств и медицинских изделий, лабораторных или клинических (медицинских) испытаний, характеризующих их качество, безопасность и эффективность), осуществление которых является обязательным.
Отказ в выдаче регистрационного удостоверения по иным основаниям, в том числе по мотивам нецелесообразности, не допускается.
Уведомление об отказе в выдаче удостоверения направляется или выдается (вручается) в письменной форме с указанием причин отказа.
Если устранение причин отказа субъектом предпринимательства влечет изменение свойств лекарств и медицинских изделий, связанных с их качеством, эффективностью и безопасностью, то заявление считается вновь поданным и рассматривается Главным управлением на общих основаниях.
При повторном рассмотрении документов не допускается приведение со стороны Главного управления причин отказа, ранее не изложенных в письменной форме заявителю, за исключением тех, которые связаны с документами, удостоверяющими устранение ранее указанных причин.
Заявление, поданное по истечении срока, указанного в уведомлении об отказе в выдаче удостоверения, считается вновь поданным и рассматривается Главным управлением на общих основаниях.
В случае изменения сведений, приведенных в регистрационных документах лекарства и медицинского изделия, в течение срока действия удостоверения субъект предпринимательства обращается в Главное управление с заявлением о внесении изменений и дополнений с приложением соответствующих документов, и при необходимости представляет образцы и стандарты.
В случае преобразования субъекта предпринимательства, он либо его правопреемник обязан в течение 7 рабочих дней после прохождения перерегистрации подать в Главное управление заявление о переоформлении удостоверения с приложением документов, подтверждающих указанные сведения.
Срок действия регистрационного удостоверения может быть продлен по заявлению, поданному субъектом предпринимательства в Главное управление с приложением необходимых документов. Заявление о продлении срока действия должно быть подано в течение 3 месяцев до истечения срока его действия. Продление удостоверения осуществляется в порядке, предусмотренном для его выдачи.
Приостановление, прекращение действия и аннулирование регистрационного удостоверения производится в случаях и порядке, предусмотренных статьями 22, 23 и 25 Закона «О разрешительных процедурах в сфере предпринимательской деятельности».
|
РАЗМЕРЫ СБОРОВ
|
||
|
Вид сбора
|
Отечественные производители |
Зарубежные производители |
|
рассмотрение заявления |
10 МРЗП
|
устанавливается Министерством здравоохранения в пределах суммы расходов Главного управления на осуществление указанных процедур |
|
выдача регистрационного удостоверения |
2 МРЗП
|
|
|
рассмотрение заявления о внесении изменений и дополнений в регистрационные документы |
5 МРЗП
|
|
|
переоформление регистрационного удостоверения |
||
|
продление срока действия регистрационного удостоверения |
||
|
выдача дубликата регистрационного удостоверения |
||
Обзор «Новое в законодательстве Республики Узбекистан» подготовила
Елена ЕРМОХИНА,
наш эксперт-юрист.